2019年5月16日,国家药监局发布《国家药监局综合司公开征求<疫苗追溯基本数据集(征求意见稿)>等3项信息化标准意见》,文件包括疫苗追溯基本数据集(征求意见稿)、疫苗追溯数据交换基本技术要求(征求意见稿)、药品追溯系统基本技术要求(征求意见稿)、标准征求意见反馈表4个文件,进行为期一个月的意见征集工作。
一. 药品追溯系统基本技术要求(征求意见稿)
本标准规定了药品追溯系统(以下简称追溯系统)的通用要求、功能要求、存储要求、安全要求和运维要求等内容。
适用于指导药品上市许可持有人、生产企业、经营企业、使用单位及第三方技术机构等药品追溯体系参与方建设和使用追溯系统。
文件对药品追溯协同服务平台、药品追溯系统、药品追溯码、药品标识码给予明确。
二. 疫苗追溯基本数据集(征求意见稿)
疫苗追溯基本数据集:用于指导疫苗追溯系统的建设,规定了与疫苗追溯体系建设相关的疫苗追溯基本数据集的分类、数据提供方关系及内容。
分为两类:
基础信息数据子集包含疫苗追溯协同服务平台分发的基础数据及补充内容;
应用信息数据子集包含了疫苗在生产、流通及使用等全过程追溯信息。
三. 疫苗追溯数据交换基本技术要求(征求意见稿)
规定了疫苗追溯体系中疫苗追溯数据交换的方式、数据格式、数据内容、性能和安全的要求。适用于指导疫苗追溯各参与方进行疫苗追溯数据交换。
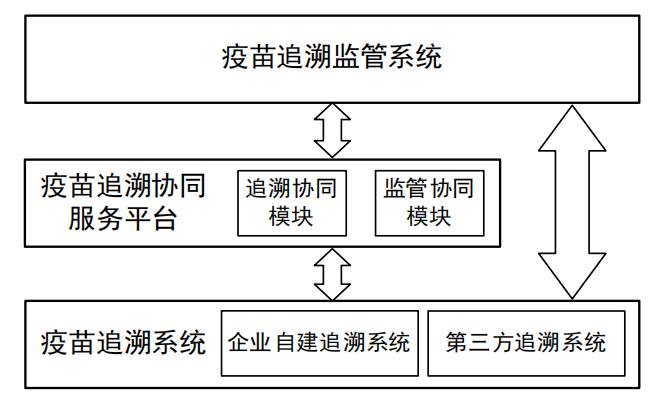
疫苗追溯数据交换是指疫苗追溯监管系统(以下简称监管系统)、疫苗追溯协同服务平台(以下简称协同平台)和疫苗追溯系统(以下简称追溯系统)相互之间进行的与追溯相关的信息交换。
趋势:
2019年4月28日,国家药监局发布《药品信息化追溯体系建设导则》《药品追溯码编码要求》两项信息化标准,紧接着昨天发布《药品追溯系统技术基本要求(征求意见稿)》,可见药品追溯信息化系列标准的编制工作不断完善,后期仍将会有相关标准的发布。同时说明药品追溯体系建设节奏已明显加快,并不断深入、细化。
单独针对疫苗建立追溯体系,充分说明国家高度重视疫苗安全。严格落实“四个最严”要求,保证疫苗产品质量与安全。
从“各数据提供方应向疫苗追溯系统提供的数据子集”表中,可以看出,疫苗上市许可人及生产企业在疫苗追溯体系中承担主体责任;
疫苗追溯数据提供方不包括配送企业,将配送方的追溯数据归到生产企业,由生产企业对配送企业进行质量安全把关,有利于明确生产企业责任主体地位,强化其质量安全管理。
随着药品追溯体系的不断完善,未来可能会彻底解决物流端和使用端的扫码率低的问题,真正实现药品全程可追溯。
快享医疗丨助力建设院内药品追溯系统
快享医疗科技(上海)有限公司隶属于卫宁健康集团旗下子公司,是一家专注于为医院提供院内第三方供应链运营管理服务的公司,我们致力于打造院内超级供应链体系,对整个医院内部物流管理进行整体运营规划,帮助医院节约药品耗材在医院流通成本,保证医院药品和耗材供应的畅通和信息资源共享。
快享医疗实现在物资单元化模式流通的基础上,对每一个流通的单元赋予唯一的身份认证,对于不同的应用场景,使用不同的条码管理方案,并结合物联网技术在关键环节的使用和识别,使院内物资耗材物流建设实现医院院内物资的全程追溯。
来源可查
通过建立与各个供应商的药品物流供应平台,实现物资耗材采购的全生命周期管理,所有采购信息、配送信息通过平台进行数据交互,后期可随时查看物资来源,做到来源可查。
去向可追
通过多条码融合平台融合药品的商品码、供应商物流码、医院的货位码等,做到精确到一颗药的全程追溯【单剂量包条码】,实现药品物流作业扫码记录,并串接软硬件,细化物流所有作业环节,实现其从药品供应商到医院大库、医院药房、医院二级库房、患者使用的全程信息追溯。


 扫一扫,关注微信
扫一扫,关注微信